Universidad de Chile
FACULTAD DE MEDICINA
ESCUELA DE Tecnología Médica
asignatura de inmunología
Apuntes
El sistema inmune: organos, células y moléculas
Prof. Inés Pepper
Los órganos
que forman parte del sistema inmune adaptativo pueden dividirse en órganos
centrales (médula ósea y timo), donde los linfocitos maduran y órganos
periféricos (ganglios linfáticos y bazo, SALT y MALT), donde los linfocitos
vírgenes son activados por antígenos.
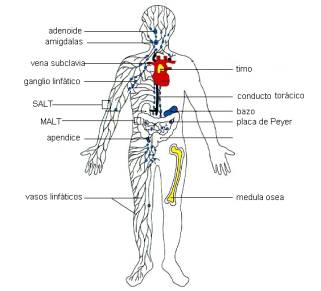
El
tejido linfoide ubicado en estos órganos tiene su origen en la médula ósea que contiene las células
troncales para todas las células hemopoyéticas y linfoides. La Médula Osea es
el sitio de maduración los linfocitos B y el timo es el órgano donde se
desarrollan los linfocitos T
Los ganglios
linfáticos son los sitios donde los linfocitos B y T responden a antígenos que
son recogidos por la linfa que drena los tejidos periféricos. Los linfocitos en
el bazo responden a antígenos transportados por la sangre. Los ganglios
linfáticos y el bazo están organizados en áreas de células B (folículos) y
áreas de células T (zonas parafoliculares). Las áreas T son también los sitios
de residencia de células dendríticas maduras, que son células accesorias
especializadas para la activación de células T vírgenes. Las células foliculares
dendríticas residen en las áreas B y sirven para activar a las células B
durante las respuestas inmunes humorales a antígenos proteicos. El desarrollo
de la arquitectura del tejido linfoide secundario depende de citoquinas.
El sistema
inmune cutáneo (SALT) consiste
células accesorias y linfocitos capaces
de responder a antígenos ambientales
que se encuentran en la piel. Una red de células dendríticas inmaduras,
llamadas células de Langerhans, está presente en la epidermis de la piel y
sirve para atrapar antígenos y luego transportarlos a los ganglios linfáticos.
También hay linfocitos T intracutáneos, que pertenecen en su mayoría a la
subpoblación gd. Estos
linfocitos tieneN una especificidad mas amplia pudiendo cada uno de ellos,
reconocer una mayor variedad de antígenos.
El
sistema inmune de las mucosas está formado
por linfocitos y células accesorias organizadas para optimizar el
encuentro con antígenos ambientales introducidos a través de los tractos
respiratorio, gastrointestinal y génito-urinario. Las placas de Peyer en la
pared intestinal y las amígdalas en la orofaringe son ejemplos de tejido del
sistema inmune de las mucosas.
La organización anatómica de las células y tejidos del sistema inmune es
ideal para conseguir la activación de linfocitos específicos para la gran
diversidad de antígenos presentes en el medio ambiente y en el interior del
organismo. Su organización permite al pequeño número de linfocitos específicos
para un antígeno cualquiera, localizar y responder efectivamente a ese antígeno,
independientemente del sitio del cuerpo donde se introdujo el antígeno.
Células que participan en la respuesta
inmune:
En la respuesta inmune adaptativa participan linfocitos
antígeno-específicos, células accesorias requeridas para la activación
linfocitaria y células efectoras que eliminan el antígeno.
Los linfocitos B y T expresan receptores para antígeno muy diversos y
específicos, y son las células responsables de la especificidad y memoria de
las respuestas inmunes adaptativas. Las células NK son una clase distinta de
linfocitos que no expresan receptores para antígeno y cuyas funciones
corresponden principalmente a la inmunidad innata. Muchas moléculas de
superficie se expresan diferencialmente en diferentes subtipos de linfocitos,
así como en otros leucocitos, los que son nominados de acuerdo a la
nomenclatura CD.
Las células B
y T vírgenes son linfocitos maduros que no han sido estimulados por antígeno
para transformarse en linfocitos diferenciados. Cuando ellos encuentran el
antígeno, se diferencian en linfocitos efectores que tienen funciones en las
respuestas inmunes protectoras. Los linfocitos B efectores son células
plasmáticas secretoras de anticuerpos. Las células T efectoras incluyen las
células T colaboradoras CD4+ secretoras de citoquinas y las células
T citotóxicas CD8+ o linfocitos T citotóxicos CTLs.
Algo de la
progenie de los linfocitos B y T activados por antígeno se diferencia en
células de memoria que sobreviven por largos períodos de tiempo en un estado de
reposo. Estas células de memoria son responsables de las respuestas rápidas y
potenciadas a subsecuentes exposiciones al antígeno.
Las células
accesorias promueven la activación de linfocitos y realizan funciones efectoras
que pueden ser potenciadas por las respuestas inmunes adaptativas humorales o
celulares. Las células accesorias incluyen fagocitos mononucleares, células
dendríticas y células foliculares dendríticas.
Una
característica importante es su constante recirculación celular entre estos
compartimentos lo cual aumenta la probabilidad de encuentro entre linfocitos y
el antígeno para el cual son específicos. Asimismo, la estructura histológica
de órganos linfoides permite la existencia de interacciones celulares
necesarias para la respuesta inmune.
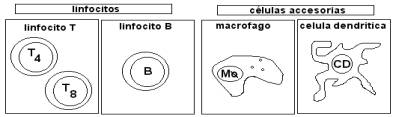
Los
linfocitos pequeños son células de 8-10 micrones de diámetro, tienen un núcleo
grande, poco citoplasma, escasas mitocondrias y carecen de organelos
especializados. De acuerdo al lugar donde se han desarrollado, los linfocitos
pueden ser T o B. Durante la ontogenia, células stem provenientes de médula
ósea viajan al timo embrionario originando los linfocitos T o bien
permanecen en la médula ósea madurando como linfocitos B. Los linfocitos
T son responsables de las respuestas efectoras celulares y de la inducción y
activación de respuestas inmunes humorales y celulares. Los linfocitos B son
las células encargadas de las respuestas humorales y las únicas capaces de
sintetizar inmunoglobulinas (Ig) de membrana. Se diferencian a células
plasmáticas las que sintetizan y secretan grandes cantidades de Ig o
anticuerpos. La función de reconocimiento específico de antígeno por parte de
linfocitos T y B se cumple mediante receptores de membrana TCR en linfocitos T
y receptores IgM e IgD en linfocitos B. Los linfocitos T pertenecen a dos
subclases: linfocitos T4 y T8 que difieren en cuanto a su función y moléculas
de superficie.
Los linfocitosT4 tienen función helper o cooperadora
durante la inducción de la respuesta y de liberación de citoquinas en la
respuesta efectora celular tipo HS retardada. Los T8 tienen función supresora
en la regulación de la respuesta y citotóxica en la fase efectora.
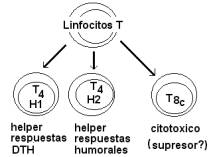
Los linfocitos T maduran en el
timo donde se diferencian constituyendo clones y subpoblaciones. Un clon está
formado por todos aquellos linfocitos que comparten una misma especificidad la
cual radica en receptores de superficie denominados TCR. Las subpoblaciones
linfocitarias se distinguen entre sí por la función que ejercen durante la
respuesta inmune. Las distintas subpoblaciones presentan diferentes moléculas
de superficie denominadas marcadores CD. Así, los linfocitos T CD4+ ejercen la
función de cooperadores o bien son liberadores de sustancias solubles
denominadas linfoquinas que interactúan con las células accesorias especialmente
macrofagos(respuesta DTH). Los linfocitos T CD8+ ejercen la función citotóxica
o según algunos autores, función supresora
Los linfocitos B inician su
maduración en la médula ósea, conformando clones que salen a la periferia con
receptores específicos para antígeno que corresponden a inmunoglobulina M unida
a membrana. A raíz de su contacto con este, los linfocitos B sufren cambios
isotípicos que los llevan a sintetizar las otras clases de inmunoglobulinas
,las que secretan luego de diferenciarse a células plasmáticas.
De este modo, los linfocitos B
conforman subpoblaciones capaces de responder con una de cinco clases de
inmunoglobulinas de una determinada especificidad: IgM, IgG, IgA, IgD e IgE . Las
inmunoglobulinas neutralizan al antígeno y activan al complemento durante la
respuesta efectora.
Las inmunoglobulinas se denominan tambien
anticuerpos.
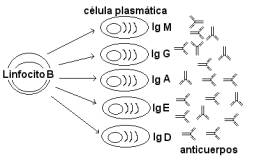
Los
linfocitos T CD4+ reconocen a los determinantes antigénicos en el contexto de
moléculas MHC clase II en la membrana de las células presentadoras de antígeno.
Los linfocitos T CD8+ reconocen al antígeno presentado por moléculas MHC clase
I ubicadas en la superficie de cualquier célula nucleada. Los linfocitos B lo
hacen directamente a través de su receptor idiotípico.
Un tercer grupo de linfocitos corresponden a las
celulas nulas, linfocitos grandes granulares o celulas NK (natural killer). Estas
no tienen marcadores T o B y su actividad consiste en lisar células
especialmente aquellas infectadas por virus o tumorales sin requerir de
reconocimiento específico del antígeno.
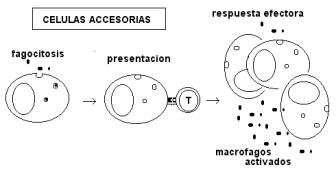
Las
células accesorias son los monocitos, macrófagos, células dendríticas, células
de Langerhans, cuya función principal es la de presentar los determinantes
antigénicos a los linfocitos T. Las células accesorias participan en la inducción
de la respuesta presentando al antígeno y en su fase efectora, amplificando la
labor de los linfocitos y eliminando al antígeno por fagocitosis. Este último
mecanismo es inespecífico, ya que no discrimina entre distintos antígenos. Sin
embargo, su eficiencia aumenta grandemente al reconocer el fragmento Fc de
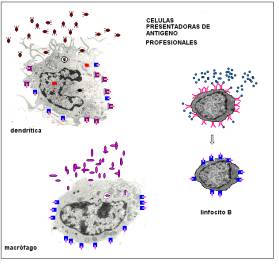
inmunoglobulinas que recubren al antígeno(opsoninas). Las células accesorias
más importantes son las células presentadoras de antígeno, que corresponden a
macrófagos, células dendríticas, células interdigitantes, células de Langerhans
y células endoteliales entre otras. Estas células están ampliamente
distribuidas en el organismo especialmente en los órganos linfoides
periféricos, ganglios y bazo, donde captan, procesan y presentan a los determinantes
antigénicos a los linfocitos T. Especial importancia tienen las células de
Langerhans, ubicadas en la epidermis, que presentan antígenos que ingresan por
esa vía y los macrófagos ubicados en las mucosas. Estas células forman parte
del sistema linfoide asociado a piel (SALT) y a mucosas (MALT) respectivamente.
Las células endoteliales han surgido últimamente como importantes participantes
en la respuesta inmune al tener capacidad de presentar antígenos, de secretar
citoquinas y de exponer moléculas de adhesión celular que otorgan
direccionalidad a la migración y ubicación de las células en los lugares donde
son requeridas. Los linfocitos B también tienen la capacidad de presentar
antígeno.
Durante
la respuesta inmune, se produce una serie de interacciones entre las células
linfoides y no linfoides que en ella participan. Estas interacciones son por
contacto directo de las células involucradas o por liberacion de citoquinas,
sustancias solubles que llevan determinados mensajes entre una y otra celula.
Otro tipo de linfocitos que
participan en la respuesta inmune son los linfocitos grandes granulares los
cuales no son T ni B ni tienen marcadores CD 4 u 8. Estos linfocitos son
también denominados NK (células asesinas naturales o natural killer) debido a
su capacidad de lisar células ya sea directamente o a través de la unión de sus
receptores al fragmento Fc de inmunoglobulinas que cubren a la célula a ser
eliminada. Los
linfocitos grandes granulares son de gran importancia en el fenómeno llamado
"vigilancia inmunologica" al ser los encargados de lisar células que
presentan neoantigenicidad, especialmente células cancerosas.
Finalmente, los
polimorfonucleares neutrófilos, basófilos y eosinófilos juegan un papel
importante en la respuesta inmune. Los primeros presentan un gran poder
fagocítico especialmente cuando las partículas a fagocitar están opsonizadas
con inmunoglobulinas o complemento. Los basófilos secretan mediadores químicos
de la inflamación y los eosinófilos participan especialmente en la respuesta
inmune frente a parásitos y en reacciones alérgicas.
Una característica importante de las
células que participan en la respuesta inmune es su recirculación, la cual
aumenta grandemente la probabilidad de encuentro entre el antígeno y los
linfocitos específicos para él.
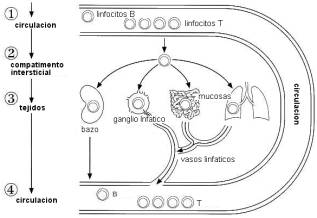
La recirculación linfocitaria es el proceso por el cual los linfocitos continuamente se mueven entre territorios de todo el cuerpo, a través de la sangre y linfáticos y es crítico para las fases de iniciación y efectora de las respuestas inmunes.
Las células
vírgenes normalmente recirculan entre los órganos linfoides periféricos,
aumentando la probabilidad de encuentro con el antígeno, que es presentado por
células presentadoras de antígeno CPAs, tales como las células dendríticas
maduras. Las células T de memoria y efectoras son preferentemente reclutadas en
sitios periféricos de inflamación donde están localizados los microorganismos.
El proceso de
recirculación linfocitaria es gobernado por moléculas de adhesión, responsables
de interacciones entre linfocitos y células endoteliales vasculares, con un patrón de recirculación que difiere
entre diferentes subtipos de linfocitos. Las moléculas de adhesión expresadas
en los linfocitos que median la recirculación se denominan receptores homing. Células endoteliales en
diferentes tejidos pueden expresar diferentes ligandos para estos receptores,
denominados adressinas que promueven el
homing tejido específico de los
linfocitos.
El homing
selectivo de las células T vírgenes en los ganglios linfáticos está mediado
principalmente por la unión de L-selectina de las células T, a adressinas de
las vénulas de endotelio alto (HEV) en los ganglios linfáticos periféricos. Las
células T de memoria y efectoras que son generadas por la estimulación antigénica
de células T vírgenes, salen del ganglio linfático. Ellas tienen una expresión
disminuida de L-selectina pero, aumentada de integrinas y ligandos de
E-selectina y P-selectina, siendo estas últimas las que median la unión al
endotelio en sitios periféricos inflamados.
Las características histológicas de los
órganos centrales y periféricos del sistema inmune aumenta la probabilidad de
encuentro entre epitopo y linfocitos con receptores específicos para él. Estos
órganos están formados por una intrincada red de células de origen epitelial o
reticular, macrófagos y células dendríticas. estas últimas tienen la capacidad
de presentar antígenos en su superficie, con o sin participación de moléculas
codificadas por MHC. Los linfocitos circulan a través de esta red celular,
teniendo oportunidad de contactar al epitopo que corresponde a su receptor
idiotípico
En los órganos linfoides centrales, timo y
médula osea, se produce la maduración y diferenciación de las células linfoides
encargadas de la respuesta inmune adaptativa. Durante la maduración los
linfocitos adquieren su especificidad idiotípica y sus características
funcionales. Los linfocitos que maduran en el timo se denominan linfocitos T y
pueden pertenecer a dos grandes subpoblaciones, los T CD4+ y los T CD8+. Son
los encargados de la respuesta celular. En médula ósea maduran los linfocitos B
que son responsables de la respuesta humoral o de anticuerpos.
Los órganos linfoides
periféricos incluyen a los numerosos ganglios linfáticos distribuidos por todo
el organismo, al bazo y a los tejidos linfoides asociados a piel (SALT) y a
mucosas (MALT).

La recirculación linfocitaria entre estos
órganos a traves de la circulación sanguínea y linfática es permanente, si bien
existen áreas en donde predominan linfocitos T o B. Los linfocitos suelen ingresar desde la sangre a los ganglios
linfáticos a traves de las vénulas de endotelio alto. En los ganglio existen
zonas donde predominan los linfocitos T (area paracortical) y otras donde se
encuentran mayoritariamente linfocitos B ( centros
germinativos en la corteza. En la medula se aprecia las células plasmáticas
productoras de anticuerpos. Los
linfocitos ubicados en órganos periféricos y aquellos recirculando por los
tejidos, pueden tomar contacto con el determinante antigénico correspondiente
iniciando la respuesta inmune adaptativa.
Moléculas que participan en la respuesta inmune.
Las moléculas de
reconocimiento en la respuesta humoral,inmunoglobulinas, se
presentan en dos formas: a) unidas a membrana de linfocitos B constituyendo el
receptor para antígeno y b) secretadas por células plasmáticas y presentes en
los fluidos orgánicos con función de anticuerpo.
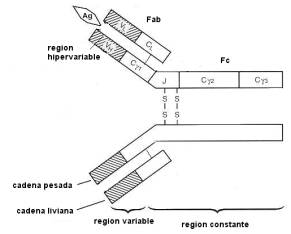
Ambas tienen una estructura básica común estando
constituidas por dos cadenas pesadas y dos cadenas livianas unidas entre si por
puentes disulfuro formando una estructura similar a un i griega. Las cadenas
pesadas y liviana presentan varios dominios, algunos de ellos constantes y uno
variable. Este ultimo está ubicado en la región aminoterminal de la cadena
Las
cadenas pesadas pueden ser de uno de cinco isotipos : m
(mu),g ( gamma),a
(alfa)
d
(delta) y e (épsilon) definiendo las cinco
clases de inmunoglobulinas IgM, IgG,
IgA, IgD e IgE respectivamente.Las cadenas livianas pueden ser l
(lambda) o k (kappa). En ambas cadenas
existen dominios constantes (4 o 5 en las pesadas y 1 en las livianas) y un
dominio variable en cada una. En el dominio variable existe una zona
hipervariable que corresponde al sitio de combinación con el antígeno; este se conoce
también como idiotipo. La molécula monomérica completa está formada por dos
cadenas livianas y dos cadenas pesadas.
Desde
el punto de vista funcional, la molécula de inmunoglobulina presenta dos
sectores, el fragmento Fc constituido por 2 dominios constantes de las cadenas
pesadasy dos fragmentos Fab constituidos por dominio constante y uno liviano de
cadena pesada y por un dominio constante y uno variable de cadena liviana El
fragmento Fc es responsable de algunas propiedades biológicas tales como activación
del complemento, opsonización, paso a través de placenta etc.. En la región Fab
se encuentra el sitio de combinación con el antígeno.
El
repertorio de anticuerpos en el
humano es de alrededor de 1012 especificidades distintas. Este
repertorio es generado durante el desarrollo de las células B por
recombinaciones en el DNA que combinan y ensamblan distintos segmentos génicos
de la región variable a partir de un grupo relativamente pequeño de secuencias
para región variable en cada locus. Este proceso es llamado recombinación
somática. Las secuencias de DNA que
codifican las regiones variables y constantes de las inmunoglobulinas están
bastante separadas en el genoma de todas las células excepto en los linfocitos
B en los cuales se han acercado a raíz de las recombinaciones nombradas que
ocurren durante el desarrollo. La diversidad aumenta más aún por el proceso de
hipermutación somática en células B maduras..
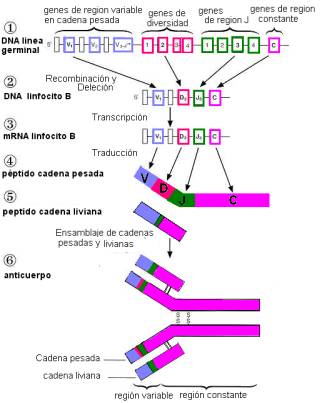
La selección al azar de los segmentos génicos para la región
variable se fija en el genoma de manera que toda la progenie de un determinado
linfocito B va a tener una sóla especificidad. Los segmentos génicos que
codifican las regiones constantes de
las cadenas pesadas y que definen el isotipo o clase (IgG, IgM etc) puede
sufrir cambios después que la célula ha contactado al antígeno. Todos los
linfocitos B inician su actividad expresando IgM. Más tarde, durante la
respuesta inmune la misma región variable puede ser ensamblada a otra cadena
pesada (gamma, epsilon, delta, etc.)
Este cambio se denomina switch isotípico y es estimulado por diversas
citoquinas en el transcurso de la respuesta inmune. La ventaja de este fenómeno
es que se obtiene inmunoglobulinas de una misma especificidad con las distintas
funciones biológicas que son en resumen las siguientes:
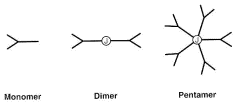
La IgM
está formada por cinco unidades básicas de inmunoglobulina unidas entre si por
una pieza J y se encuentra presente en el plasma. Tiene diez sitios de unión
con antígeno y es secretada principalmente en respuestas humorales primarias
timodependientes y en respuestas timoindependientes.
Es de baja afinidad pero presenta gran avidez por antígenos multivalentes
especialmente bacterianos. Es una potente fijadora del complemento, al
presentar cinco fragmentos Fc que unen al factor del complemento C1q. La IgM se
encuentra también en la membrana de linfocitos B en forma de monómero,
constituyendo los receptores
idiotípicos de estas células.
La IgG es la inmunoglobulina más
abundante en el plasma, es monomérica y es producida en grandes cantidades
durante respuestas secundarias a antígenos timodependientes. Sus principales
funciones biológicas incluyen fijación del complemento, unión a receptores para
Fc en células fagocíticas al opsonizar partículas durante la fogocitosis y
unión a receptores en células NK durante la citotoxicidad mediada por
anticuerpos (ADCC). Esta inmunoglobulina atraviesa la placenta confiriendo
protección al feto durante el embarazo.
La IgA se encuentra en lágrimas, leche, saliva y mucosa de los
tractos intestinal y digestivo. Está formada por dos unidades básicas unidas
por una pieza secretora sintetizada por las células epiteliales de las mucosas.
Esta pieza secretora es un polipéptido responsable del trasporte de la IgA a
través del epitelio. Ademas la proteje de la acción de enzimas proteolíticas
presentes en las secresiones. Es sintetizada en grandes cantidades por acúmulos
linfoides y placas de Peyer del intestino. No fija complemento ni es opsonina,
sin embargo su importancia es enorme al impedir el ingreso de microorganismos y
macromoléculas al organismo.
La IgE se encuentra en muy bajas
concentraciones en el suero de personas normales, y en mayores concentraciones
en individuos atópicos. En estos últimos es responsable de los cuadros de
hipersensibilidad mediada por un mecanismo de daño inmunológico tipo I de la
clasificación de Gell y Coombs. El fragmento Fc de estas inmunoglobulinas
presenta gran afinidad por receptores para Fc epsilon en células cebadas y
basófilos. Al estar ubicada en su superficie y recibir el estímulo antigénico,
la IgE induce su degranulación iniciando un proceso inflamatorio y produciendo
la contracción del músculo liso. En condiciones normales, esta inmunoglobulina
interviene en la respuesta inmune protectora contra parásitos especialmente
helmintos.
La IgD es una inmunoglobulina unida a
membrana de los linfocitos B. Su presencia en conjunto con IgM confiere
inmunocompetencia a estos linfocitos. Está prácticamente ausente en el suero.
Moléculas de
reconocimiento en la respuesta celular: TCR:
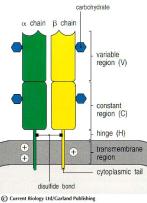
En
cuanto a los receptores presentes en linfocitos T, (TCR) se puede afirmar que
los mecanismos genéticos responsables de la diversidad idiotípica son similares
a los descritos para las inmunoglobulinas. El TCR es un heterodimero formado
por dos cadenas glicoproteicas de transmembrana alfa y beta. La porción externa
de cada cadena consiste en dos dominios, parecidos a los dominios variable y
constante de inmunoglobulinas Existen cerca de 30 000 de estas moléculas
altamente polimórficas en la superficie de cada linfocito T , todos ellos de
una misma especificidad.
Los linfocitos T reconocen determinantes antigénicos en la forma de
cadenas polipeptídicas de 10 a 20 aminoácidos presentados en la molécula MHC
clase II ubicadas en la membrana de células presentadoras de antígeno (los
linfocitos T CD4+ ) o en MHC clase I en todas las células nucleadas (los
linfocitos T CD8+ ). Para ello utilizan as
moléculas de membrana denominadas receptores para antígeno ( TCR ) también
llamado receptor idiotípico. Cada linfocito maduro expresa receptores de
una sóla especificidad, vale decir capaz de reconocer una sóla conformación
MHC-péptido antigénico. Los individuos tienen en su organismo linfocitos
con receptores con especificidad para reconocer alrededor de 1012
conformaciones diferentes. Un grupo de linfocitos que comparte la misma
especificidad se denomina clon
linfocitario. La respuesta inmune se inicia cuando estos linfocitos
contactan al complejo antígeno-MHC clase I oII ubicados en la superficie de una
celula o una CPA.respectivamente La estructura molecular de los TCR les permite
llevar a cabo la función de reconocimiento antigénico.
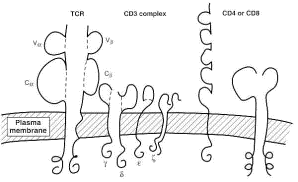
El TCR
está contiguo al complejo CD3 que es un transductor de la señal de activación y
presenta la molecula CD4 o la molecula CD8 las que determina si reconoce
antígeno en el contexto de MHC clase II o I respectivamente. Además participan moléculas de
adhesión.
Moleculas codificadas por el Complejo Mayor de Histocompatibilidad
Los antígenos
procesados son reconocidos por los linfocitos T al ser presentados por por
cualquier célula nucleada en MHC clase I o por las células presentadoras de
antígeno en moléculas MHC clase II .
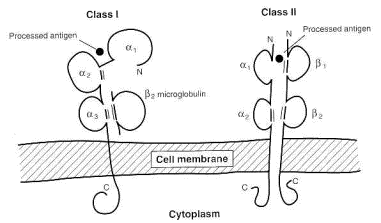
Las moléculas MHC clase I también llamadas moléculas o antígenos de
histocompatibilidad incluyen las moléculas ( y genes) HLA-A, HLA-B y HLA-C y
están ubicadas en todas las células nucleadas otorgando la "identidad
macromolecular" al individuo. Su función es presentar fragmentos
antigénicos procesados (péptidos antigénicos) a linfocitos T CD8+ o citotóxicos.
Estos antígenos se denominan también antígenos endógenos ya que son
sintetizados en la célula que los presenta.. De esta manera otorgan restricción
genética clase I a la respuesta celular citotóxica. Esto quiere decir que los
linfocitos T citotóxicos de un individuo lisan células propias que presenten
antígeno propio alterado (por ejemplo, células cancerosas) o antígenos ajenos
(por ejemplo, antígenos virales en células infectadas por virus).
Las moléculas MHC clase II incluyen las moléculas HLA-DR, HLA-DQ y
HLA-DP y están presentes en células que participan en la respuesta inmune
particularmente linfocitos B, macrófagos y otras células presentadoras de
antígeno ( CPA ). Su función es presentar antígenos procesados, también
denominados antígenos exógenos, a linfocitos T CD4+. Son necesarios para una
interacción efectiva entre células pertenecientes al sistema inmune. De esta
manera, los linfocitos T CD4+ reconocen "lo propio" ( HLA ) alterado
por un péptido antigénico ajeno.
Las moléculas clase III incluyen a los fragmentos C2 y C4 del complemento pertenecientes a la
vía clásica y a la proteína B de la vía alterna del complemento. También
codifican las citoquinas factor de necrosis tumoral (TNF) y linfotoxina (LT).
Los genes del MHC son
extraordinariamente polimórficos contando con más de cuarenta alelos para cada
gen individual. La organización de este complejo génico permite que un
individuo heterocigoto exprese seis alelos polimórficos clase II y más de seis
alelos clase I en cada célula que lo posee. (Ver clase anterior)
Moléculas CD.
Son moléculas ubicadas en la superficie de
los linfocitos cuyas funciones son principalmente: promover interacciones
célula-célula, permitir la adhesión celular y actuar como moléculas de
transducción de señales durante la activación.
Hasta 1989 se habían descrito 78 moléculas CD
ubicadas en linfocitos T, linfocitos B, monocitos, granulocitos, plaquetas etc.
Las más importantes en relación a esta revisión son:
CD 4 en linfocitos T
cooperadores reconocen MHC clase II
CD 8 en linfocitos T
citotóxicos reconocen MHC clase I
CD 3 en linfocitos T transduce
señales de activación en el
econocimiento por parte de linfocitos T
CD 2 en linfocitos T y células
NK participa en adhesión celular
CD19 en linfocitos B participa
en su activación y regulación.
Citoquinas : son hormonas peptídicas que participan en la activacion de los
linfocitos enviando señales de proliferacion y diferenciación. Las principales
son las interleuquina 2 (IL-2), 4 (IL-4) y el factor de crecimiento
transformante beta (TGF-ß).
Las citoquinas que participan
en la respuesta inmune efectora son el Interferón gamma (IFN-g), la
linfotoxina(LT), la interleuquina 5 (IL-5) y el Factor Inhibidor de la
migración de macrófagos (MIF).